Contexte
De nombreuses études ont montré que les acides gras oméga-3 (OM3), en particulier l'acide eicosapentaénoïque (EPA) et l'acide docosahexaénoïque (DHA), ont de nombreux bienfaits pour la santé, notamment pour la santé cardiovasculaire. (1-9) Cependant, la biodisponibilité et l'efficacité clinique des suppléments d'oméga-3 dépendent de divers facteurs, notamment de la forme de l'oméga-3, des effets de la matrice alimentaire et de la capacité métabolique de chaque individu. Les formes les plus courantes de suppléments d'oméga-3 sur le marché sont estérifiées en triglycérides (TG) ou en esters éthyliques (EE); cependant, ces formes ont montré des taux d'absorption plus faibles et peuvent provoquer des effets secondaires gastro-intestinaux. (10-13)
Une étude mesurant les niveaux de l'indice oméga-3 dans la population canadienne a révélé que la majorité des adultes canadiens ont un indice oméga-3 inférieur au niveau recommandé de 8%. De plus, des études suggèrent que les personnes obèses ont des niveaux d'indice oméga-3 encore plus bas, ce qui souligne l'importance de la supplémentation en oméga-3 dans la population, en particulier chez les personnes obèses ou présentant des problèmes de malabsorption des lipides. (14)
Des études récentes ont montré que la forme monoglycéride (MAG) de l'oméga-3 (MAG-O3™) est un transporteur plus efficace de l'oméga-3 par rapport aux formes TG et EE, en particulier pour les populations souffrant de malabsorption des lipides ou d'obésité.
Biodisponibilité dans une population en bonne santé
Étude clinique de biodisponibilité 1
La première étude, un essai croisé randomisé en double aveugle, a comparé la pharmacocinétique des suppléments d'oméga-3 sous forme de monoacylglycérol ou d'ester éthylique chez l'homme. L'étude a révélé qu'après avoir reçu la forme MAG (MAG-O3™), les concentrations plasmatiques d'EPA et de DHA ont atteint un pic 3 et 2,5 fois plus élevé, respectivement, par rapport à la forme EE. Lorsqu'ils étaient fournis sous forme de MAG, la concentration plasmatique d'oméga-3 pendant la phase d'absorption était en moyenne de 3 à 5 fois plus élevée que dans la forme EE. Lorsque les oméga-3 étaient fournis sous forme estérifiée dans du MAG, leur concentration 24 heures après la prise était plus élevée que dans la forme EE. L'étude a conclu que la concentration plasmatique de DHA et d'EPA était plus élevée lorsqu'ils étaient fournis sous forme de MAG (MAG-O3™) que sous forme d'EE. (15)
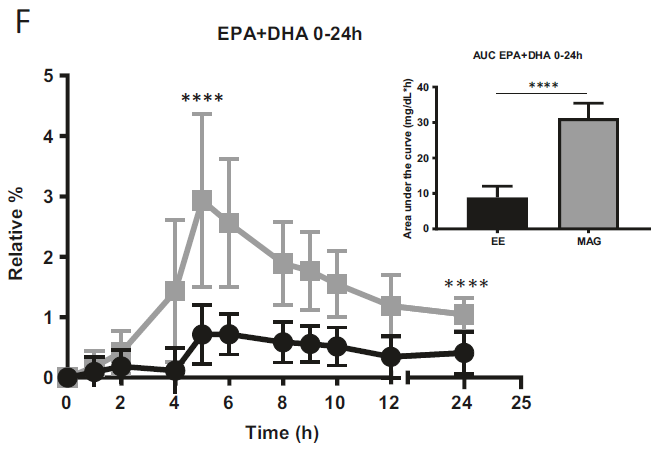
Figure 1: Pourcentage relatif d'EPA + DHA plasmatiques dans les lipides totaux sur 24 h. Tous les résultats sont exprimés en moyenne ± écart-type (n = 20).
Étude clinique de biodisponibilité 2
La deuxième étude, un essai croisé randomisé en double aveugle, a comparé l'aire sous la courbe (AUC) de 24 heures des concentrations plasmatiques d'EPA, de DHA et d'EPA+DHA lorsque ces acides gras étaient estérifiés sous forme de monoglycérides (MAGs), d'EE ou de TG (résultats primaires), et a évalué leurs effets secondaires sur 24 heures. L'étude a révélé que l'AUC de 24 heures de l'EPA plasmatique était environ 2 fois plus élevée après la prise de MAG par rapport aux formes EE et TG d'oméga-3, respectivement. L'étude a conclu que la concentration plasmatique d'acides gras OM3 chez les adultes est plus élevée après la supplémentation en acides gras oméga-3 estérifiés sous forme de MAGs plutôt que sous forme d'EE ou de TG, suggérant qu'avec une dose inférieure d'acides gras oméga-3 sous forme de MAG (MAG-O3™), les concentrations plasmatiques d'acides gras oméga-3 atteintes sont similaires à celles obtenues avec des doses plus élevées d'acides gras oméga-3 estérifiés sous forme d'EE ou de TG. (16)
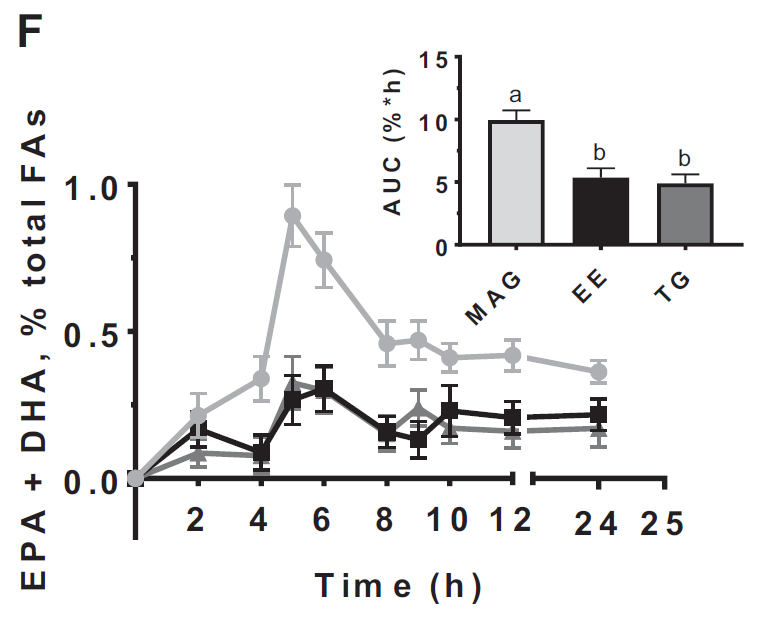
Figure 2: Concentrations plasmatiques relatives d'EPA+DHA chez les adultes pendant les 24 heures suivant la prise de suppléments de MAG, d'EE et de TG d'acides gras n-3.
Étude clinique de biodisponibilité 3
La troisième étude, un essai randomisé, a évalué l'impact de trois formes différentes d'huile de poisson (EE, rTG et MAG) sur l'indice oméga-3 après 8 semaines de supplémentation quotidienne. L'étude a révélé que l'indice oméga-3 après 8 semaines était de 8,5 pour le groupe de monoglycérides (MAG-O3™), de 7,7 pour le groupe de triglycérides réestérifiés (rTG) et de 7,1 pour le groupe d'ester éthylique (EE). L'étude a conclu que l'indice oméga-3 est plus élevé après une supplémentation quotidienne de 8 semaines en acides gras oméga-3 estérifiés sous forme de monoglycérides (MAG-O3™) plutôt que sous forme d'EE ou de rTG. Seul le groupe de monoglycérides (MAG-O3) a réussi à atteindre un indice oméga-3 de 8,0 avec une dose quotidienne de 1,3 g d'EPA+DHA. (17)
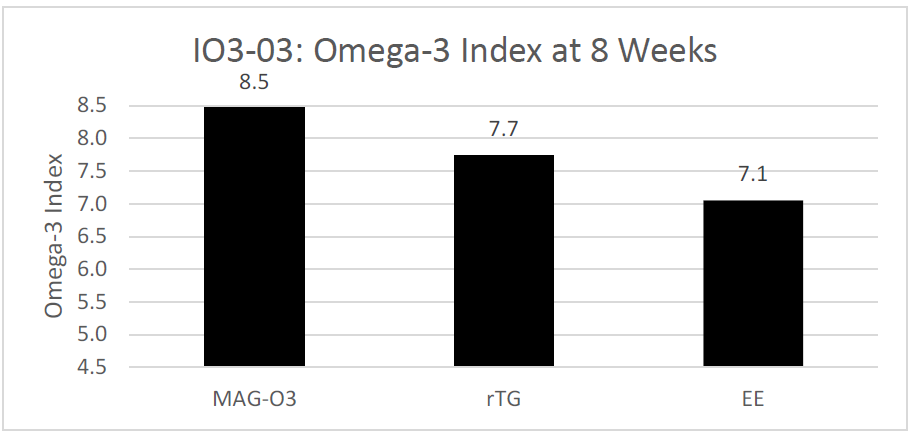
Figure 3: Niveaux d'index oméga-3 dans les globules rouges (index oméga-3) après 8 semaines de supplémentation en MAG-O3™, en EE et en TAG d'EPA et de DHA. Les résultats sont exprimés en %.
Études cliniques dans une population présentant une malabsorption des lipides ou une obésité
Étude clinique de biodisponibilité 4
La quatrième étude, un essai clinique en double aveugle, a examiné l'accumulation d'EPA (500 mg/jour) et de DHA (300 mg/jour) lorsqu'ils étaient consommés sous forme de TAG ou de MAG (MAG-O3™), dans les érythrocytes, le plasma et les chylomicrons de 45 volontaires obèses (IMC ≥30 kg/m2 et ≤40 kg/m2) qui ont reçu ou non de l'orlistat, un inhibiteur des lipases pancréatiques. L'étude a révélé que la consommation d'huile enrichie en MAG (MAG-O3™) entraînait une plus grande accumulation d'oméga-3 par rapport au TAG, les concentrations d'EPA et de DHA dans les érythrocytes étant respectivement de 72% et 24% plus élevées à 21 jours (P < 0,001). De plus, le MAG-O3™ a augmenté la concentration plasmatique d'EPA de 56% (P < 0,001) par rapport au TAG. Dans les chylomicrons, l'apport de MAG a entraîné des niveaux plus élevés d'EPA, l'aire sous la courbe (0-10 h) de l'EPA étant supérieure de 55% (P = 0,012). Ces résultats indiquent que chez les sujets obèses présentant des conditions de maldigestion/malabsorption des lipides induites par l'orlistat, l'huile de MAG LC-PUFA augmente davantage les niveaux de LC-PUFA dans les érythrocytes, le plasma et les chylomicrons que le TAG. L'étude conclut que l'huile de MAG (MAG-O3™) pourrait nécessiter une digestion enzymatique minimale avant d'être absorbée par l'intestin et transférée à travers la barrière épithéliale. (18)
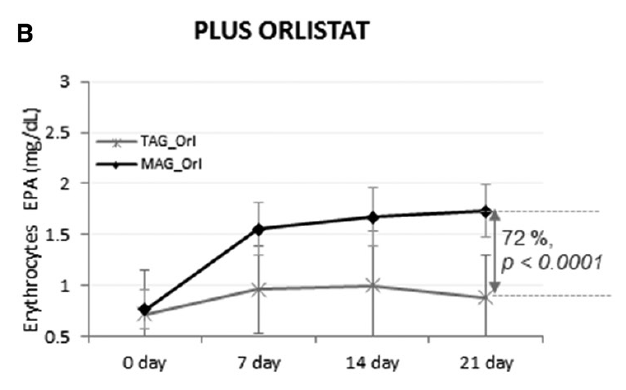
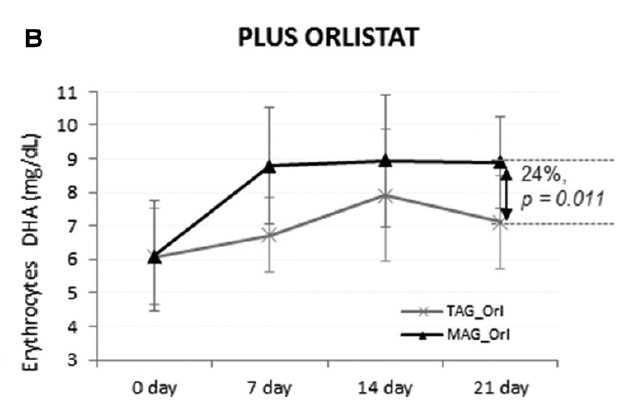
Figure 4: Accrétion des LC-PUFA aux jours 0, 7, 14 et 21. Contenu en EPA et DHA après supplémentation en huile enrichie en MAG et en TAG chez les obèses avec orlistat. Les résultats sont exprimés en mg/mL.
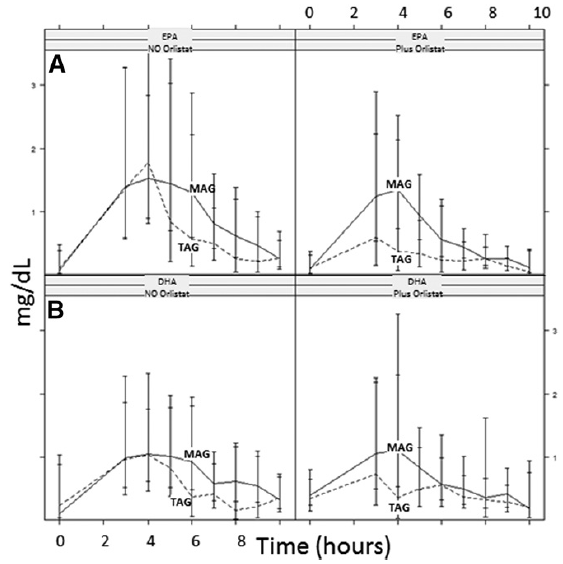
Figure 5: Effet aigu : résultats pharmacocinétiques, EPA (A) et DHA
(B) dans les chylomicrons, AUC sur 10 heures postprandiales. Les résultats sont exprimés en milligrammes par décilitre × heures.
Étude clinique de biodisponibilité 5
La cinquième étude a exploré la biodisponibilité du MAG-O3™ chez des sujets humains présentant différentes capacités métaboliques, et comment elle se comparait à d'autres formes d'oméga-3. Premièrement, les auteurs ont cherché à démontrer que l'huile de monoacylglycérol sn-1(3) (MAG-O3™) pourrait être plus biodisponible que les esters éthyliques et les acides gras libres (OM3-FFA) chez des sujets sains suivant un régime pauvre en matières grasses (essai clinique A). Deuxièmement, la biodisponibilité du MAG a été comparée à celle de l'huile de TAG chez des sujets en surpoids/obèses suivant un régime pauvre en matières grasses en mesurant les niveaux de DHA/EPA dans le plasma sanguin (essai clinique B). Troisièmement, les biodisponibilités des huiles de MAG et de TAG ont été comparées chez des patients atteints de fibrose kystique présentant une insuffisance pancréatique exocrine connue. L'absorption des LC-PUFA a été comparée en mesurant les niveaux de DHA et d'EPA dans le plasma et les érythrocytes (essai clinique C).
Les auteurs montrent chez l'homme qu'une structure lipidique d'oméga-3-sn-1(3)-monoacylglycérol "pré-digérée" (MAG-O3™) est significativement plus absorbée à des doses thérapeutiques élevées (2,9 g/jour) que la forme d'oméga-3 la plus courante, l'ester éthylique (3,1 g/jour) (utilisée pour le traitement de l'hypertriglycéridémie), et présente un profil comparable à celui des autres acides gras oméga-3 pré-digérés sous forme d'acides gras libres (OM3-FFA) (3,2 g/jour). Les doses de suppléments nutritionnels de MAG ont entraîné des augmentations similaires des niveaux d'oméga-3 dans le sang, comparées aux suppléments de triacylglycérols d'oméga-3 (OM3-TAG) chez les sujets obèses (1,2 g/jour) suivant un régime pauvre en matières grasses, et chez les enfants atteints de fibrose kystique (1,0 g/jour). Ces résultats suggèrent que les deux formes de MAG-O3™ pré-digéré et d'OM3-FFA sont absorbées efficacement et réincorporées efficacement dans les triacylglycérols à l'intérieur des entérocytes, avant d'être exportées vers le système de transport lipidique des chylomicrons. L'étude conclut que le MAG-O3™ pré-digéré pourrait fournir une thérapie plus efficace dans les cas de maladies cardiovasculaires graves nécessitant des doses élevées d'oméga-3 et un régime pauvre en matières grasses, limitant l'activité lipasique digestive. (19)
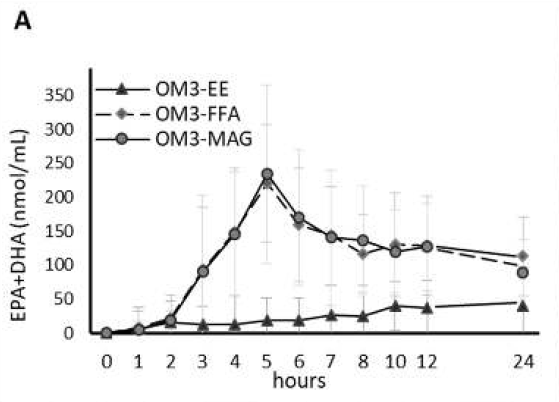
Figure 6: Essai clinique A : Population en bonne santé. Effet aigu : résultats pharmacocinétiques (corrigés par rapport à la ligne de base), EPA + DHA dans le plasma, AUC sur 24 heures postprandiales.
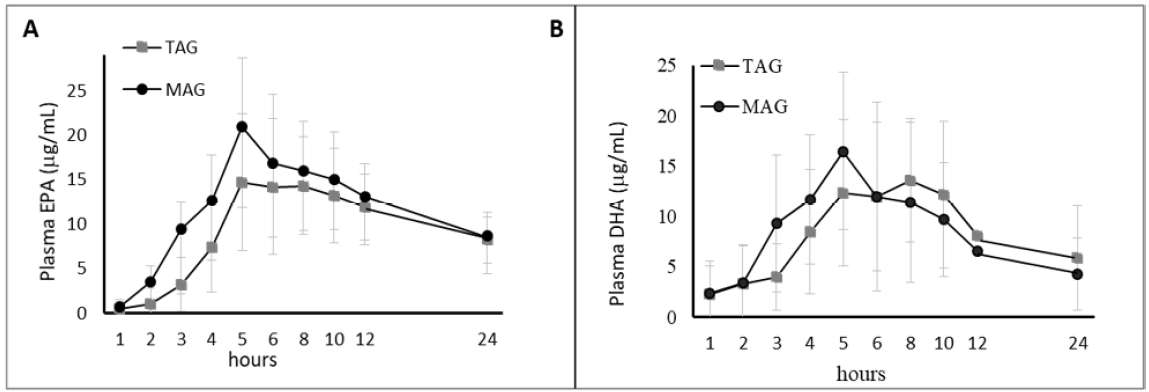
Figure 7: Essai clinique B : Population obèse. Effet aigu : résultats pharmacocinétiques (corrigés par rapport à la ligne de base), EPA (A) + DHA (B) dans le plasma, AUC sur 24 heures postprandiales (panneau supérieur). Les résultats sont exprimés en µg/mL.
Conclusion
En conclusion, ces études fournissent des preuves solides que la forme de MAG des oméga-3 (MAG-O3™) est un transporteur plus efficace des oméga-3 par rapport aux formes de TG et d'EE, en particulier pour les populations présentant une malabsorption des lipides ou une obésité. La forme de MAG des oméga-3 a montré des taux d'absorption plus élevés et une plus grande efficacité pour augmenter l'indice oméga-3, un facteur de risque de maladie coronarienne. De plus, la forme de MAG des oméga-3 présente des effets secondaires similaires ou moins nombreux par rapport aux formes d'EE et de TG. Étant donné les bienfaits pour la santé des oméga-3, les professionnels de santé devraient envisager de recommander des suppléments d'oméga-3 à base de monoglycérides (MAG-O3™) comme forme de supplémentation en oméga-3 à leurs patients.
Références
1. Musa-Veloso K, Binns MA, Kocenas AC, Poon T, Elliot JA, Rice H, Oppedal-Olsen H, Lloyd H, Lemke S. Long-chain omega-3 fatty acids eicosapentaenoic acid and docosahexaenoic acid dose-dependently reduce fasting serum triglycerides. Nutr Rev. 2010 Mar;68(3):155-67. doi: 10.1111/j.1753-4887.2010.00272.x. PMID: 20384846. (link)
2. Yokoyama, M.; Origasa, H.; Matsuzaki, M.; Matsuzawa, Y.; Saito, Y.; Ishikawa, Y.; Oikawa, S.; Sasaki, J.; Hishida, H.; Itakura, H.; et al. EPA lipid intervention study (JELIS) Investigators. Effects of eicosapentaenoic acid on major coronary events in hypercholesterolaemic patients (JELIS): A randomised open-label, blinded endpoint analysis. Lancet 2007, 369, 1090–1098. (link)
3. Mozaffarian, D.; Lemaitre, R.N.; King, I.B.; Song, X.; Huang, H.; Sacks, F.M.; Rimm, E.B.; Wang, M.; Siscovick, D.S. Plasma phospholipid long-chain omega-3 fatty acids and total and cause-specific mortality in older adults: A cohort study. Ann. Intern. Med. 2013, 158, 515–525. (link)
4. Davidson, M.H.; Stein, E.A.; Bays, H.E.; Maki, K.C.; Doyle, R.T.; Shalwitz, R.A.; Ballantyne, C.M.; Ginsberg, H.N. COMBination of prescription Omega-3 with Simvastatin (COMBOS) Investigators. Effcacy and tolerability of adding prescription omega-3 fatty acids 4 g/d to simvastatin 40mg/d in hypertriglyceridemic patients: An 8-week, randomized, double-blind, placebo-controlled study. Clin. Ther. 2007, 29, 1354–1367. (link)
5. Bays, H.E.; Tighe, A.P.; Sadovsky, R.; Davidson, M.H. Prescription omega-3 fatty acids and their lipid effects: Physiologic mechanisms of action and clinical implications. Expert Rev. Cardiovasc. Ther. 2008, 6, 391–409. (link)
6. Oman, E.; Marenco, T.; Ferber, S.; Johnson, J.; Kling, D.; Curcio, D.; Davidson, M. Steady-state bioavailability of prescription omega-3 on a low-fat diet is significantly improved with a free fatty acid formulation compared with an ethyl ester formulation: The ECLIPSE II study. Vasc. Health Risk Manag. 2013, 9, 563–573. (link)
7. Laidlaw, M.; Cockerline, C.A.; Rowe, W.J. A Randomized clinical trial to determine the effcacy of manufacturers’ recommended doses of omega-3 fatty acids from different sources in facilitating cardiovascular disease risk reduction. Lipids Health Dis. 2014, 13, 1–13. (link)
8. Chowdhury, R.; Warnakula, S.; Kunutsor, S.; Crowe, F.; Ward, H.A.; Johnson, L.; Franco, O.H.; Butterworth, A.S.; Forouhi, N.G.; Thompson, S.G.; et al. Association of dietary, circulating, and supplement fatty acids with coronary risk: A systematic review and meta-analysis. Ann. Intern. Med. 2014, 160, 398–406. (link)
9. Maki, K.C.; Palacios, O.M.; Bell, M.; Toth, P.P. Use of supplemental long-chain omega-3 fatty acids and risk for cardiac death: An updated meta-analysis and review of research gaps. J. Clin. Lipidol. 2017, 11, 1152–1160.e2. (link)
10. Mu, H., and C. E. Høy. 2004. The digestion of dietary triacylglycerols. Prog. Lipid Res. 43: 105–133. (link)
11. Christensen, M. S., C. E. Høy, C. C. Becker, and T. G. Redgrave. 1995. Intestinal absorption and lymphatic transport of eicosapentaenoic (EPA), docosahexaenoic (DHA), and decanoic acids: dependence on intramolecular triacylglycerol structure. Am. J. Clin. Nutr. 61: 56–61. (link)
12. Innis, S. M., and R. Dyer. 1997. Dietary triacylglycerols with palmitic acid (16:0) in the 2-position increase 16:0 in the 2-position of plasma and chylomicron triacylglycerols, but reduce phospholipid arachidonic and docosahexaenoic acids, and alter cholesteryl ester metabolism in formula-Fed piglets. J. Nutr. 127: 1311–1319. (link)
13. Valenzuela, A., V. Valenzuela, J. Sanhueza, and S. Nieto. 2005. Effect of supplementation with docosahexaenoic acid ethyl ester and sn-2 docosahexaenyl monoacylglyceride on plasma and erythrocyte fatty acids in rats. Ann. Nutr. Metab. 49: 49–53. (link)
14. Langlois K, Ratnayake WM. Omega-3 Index of Canadian adults. Health Rep. 2015 Nov;26(11):3-11. PMID: 26583692. (link)
15. Chevalier L, Plourde M. Comparison of pharmacokinetics of omega-3 fatty acid supplements in monoacylglycerol or ethyl ester in humans: a randomized controlled trial. Eur J Clin Nutr. 2021 Apr;75(4):680-688. doi: 10.1038/s41430-020-00767-4. Epub 2020 Oct 3. PMID: 33011737; PMCID: PMC8035073. (link)
16. Chevalier L, Vachon A, Plourde M. Pharmacokinetics of Supplemental Omega-3 Fatty Acids Esterified in Monoglycerides, Ethyl Esters, or Triglycerides in Adults in a Randomized Crossover Trial. J Nutr. 2021 May 11;151(5):1111-1118. doi: 10.1093/jn/nxaa458. PMID: 33564872; PMCID: PMC8112767. (link)
17. Unpublished Comparative human pilot study evaluating three different fish oil forms and their impact on the Omega-3 index.
https://clinicaltrials.gov/ct2/show/NCT04159532?term=NCT04159532&draw=2&rank=1
18. Cruz-Hernandez C, Destaillats F, Thakkar SK, Goulet L, Wynn E, Grathwohl D, Roessle C, de Giorgi S, Tappy L, Giuffrida F, Giusti V. Monoacylglycerol-enriched oil increases EPA/DHA delivery to circulatory system in humans with induced lipid malabsorption conditions. J Lipid Res. 2016 Dec;57(12):2208-2216. doi: 10.1194/jlr.P070144. Epub 2016 Oct 5. PMID: 27707818; PMCID: PMC5321218. (link)
19. Cuenoud B, Rochat I, Gosoniu ML, Dupuis L, Berk E, Jaudszus A, Mainz JG, Hafen G, Beaumont M, Cruz-Hernandez C. Monoacylglycerol Form of Omega-3s Improves Its Bioavailability in Humans Compared to Other Forms. Nutrients. 2020 Apr 7;12(4):1014. doi: 10.3390/nu12041014. PMID: 32272659; PMCID: PMC7230359. (link)